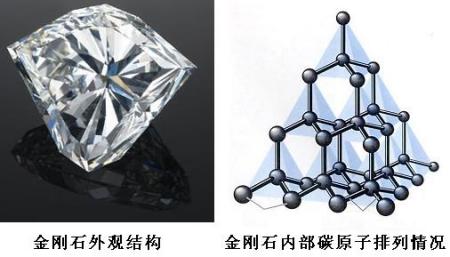
一、石墨与金刚石的熔点哪个高??为什麽?
金刚石的熔点是3550℃,石墨的熔点是3652℃~3697℃(升华)。石墨熔点高于金刚石。
从片层内部来看,石墨是原子晶体;从片层之间来看,石墨是分子晶体(总体说来,石墨应该是混合型晶体);而金刚石是原子晶体。石墨晶体的熔点反而高于金刚石,似乎不可思议,但石墨晶体片层内共价键的键长是1.42×10-10m,金刚石晶体内共价键的键长是1.55×10-10m。同为共价键,键长越小,键越牢固,破坏它也就越难,也就需要提供更多的能量,故而熔点应该更高。
(主要就是石墨的分子晶体属性导致它的熔点高)
二、金刚石与石墨谁沸点大?熔点呢?为什么?
沸点相同(4827摄氏度),但熔点确实是石墨高(金刚石熔点3550摄氏度,石墨3652摄氏度)。这是实验事实,实验中把石墨转化为金刚石的过程是吸热反应。不能简单的用晶体类型说金刚石熔点比石墨高。因为金刚石是4个C-C键,石墨是3个C-C键加高度离域的大π键,熔化要克服不同的键的键能,因此无法从这个角度上比较谁高,只能由实验测得。实践是检验真理的惟一标准!
三、金刚石和石墨熔点比较
一定是石墨熔点最高.
石墨的熔点为3850±50℃,沸点为4250℃(来源百度百科)
这似乎和硬度以及空间结构没有明显联系.
四、石墨和金刚石的熔点和沸点问题
金刚石的熔点是3550℃,石墨的熔点是3652℃~3697℃(升华)。石墨熔点高于金刚石。
从片层内部来看,石墨是原子晶体;从片层之间来看,石墨是分子晶体(总体说来,石墨应该是混合型晶体);而金刚石是原子晶体。石墨晶体的熔点反而高于金刚石,似乎不可思议,但石墨晶体片层内共价键的键长是1.42×10-10m,金刚石晶体内共价键的键长是1.55×10-10m。同为共价键,键长越小,键越牢固,破坏它也就越难,也就需要提供更多的能量,故而熔点应该更高。
(主要就是石墨的分子晶体属性导致它的熔点高)
五、石墨和金刚石,究竟谁的熔点高?
金刚石的熔点是3550℃,石墨的熔点是3652℃~3697℃(升华).石墨(石墨的分子晶体属性导致它的熔点高)熔点高于金刚石.
从片层内部来看,石墨是原子晶体;从片层之间来看,石墨是分子晶体(总体说来,石墨应该是混合型晶体);而金刚石是原子晶体.石墨晶体的熔点反而高于金刚石,似乎不可思议,但石墨晶体片层内共价键的键长是1.42×10-10m,金刚石晶体内共价键的键长是1.55×10-10m.同为共价键,键长越小,键越牢固,破坏它也就越难,也就需要提供更多的能量,故而熔点应该更高.
还要从石墨和金刚石的晶体结构着手,金刚石和石墨的本质都是碳元素.但是它们的晶体结构是不同的,况且,金刚石和石墨中的碳原子的排列顺序不同,这是照成它他们之间晶体结构不同的主要原因.金刚石中碳原子之间的碳碳键是一个碳原子分别和四个碳原子形成一个碳碳单键,每六个碳原子形成一个六元环,这个六元环的键能非常强,极难破坏,因此决定了金刚石的高熔点,高沸点性质.而石墨的碳原子是分层排布的,层与层之间的碳原子之间通过共价键连接,每一层的碳原子之间,每一个碳原子分别和四个碳原子形成一个碳碳单键,每六个碳原子形成一个六元环.但层与层之间的共价键很容易被破坏,所以,这决定了石墨的底熔点和底沸点的性质.
方法归纳:
在比较物质或元素的熔沸点的问题上,首先从它的种类上去比较.
1.同主族元素:从上到下元素的原子半径逐渐增大,容易失去最外层的电子,因此,同主族元素,从上到下元素所对应的单质,熔沸点逐渐降低.
2.同周期元素:从左到右元素的原子半径逐渐增大,所对应的单质,从左到右,熔沸点逐渐降低.
3.熔沸点:原子晶体>离子晶体>金属晶体>分子晶体